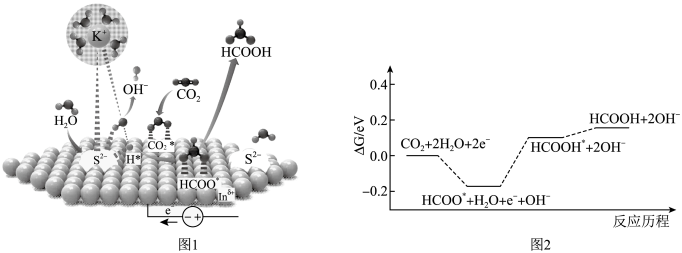
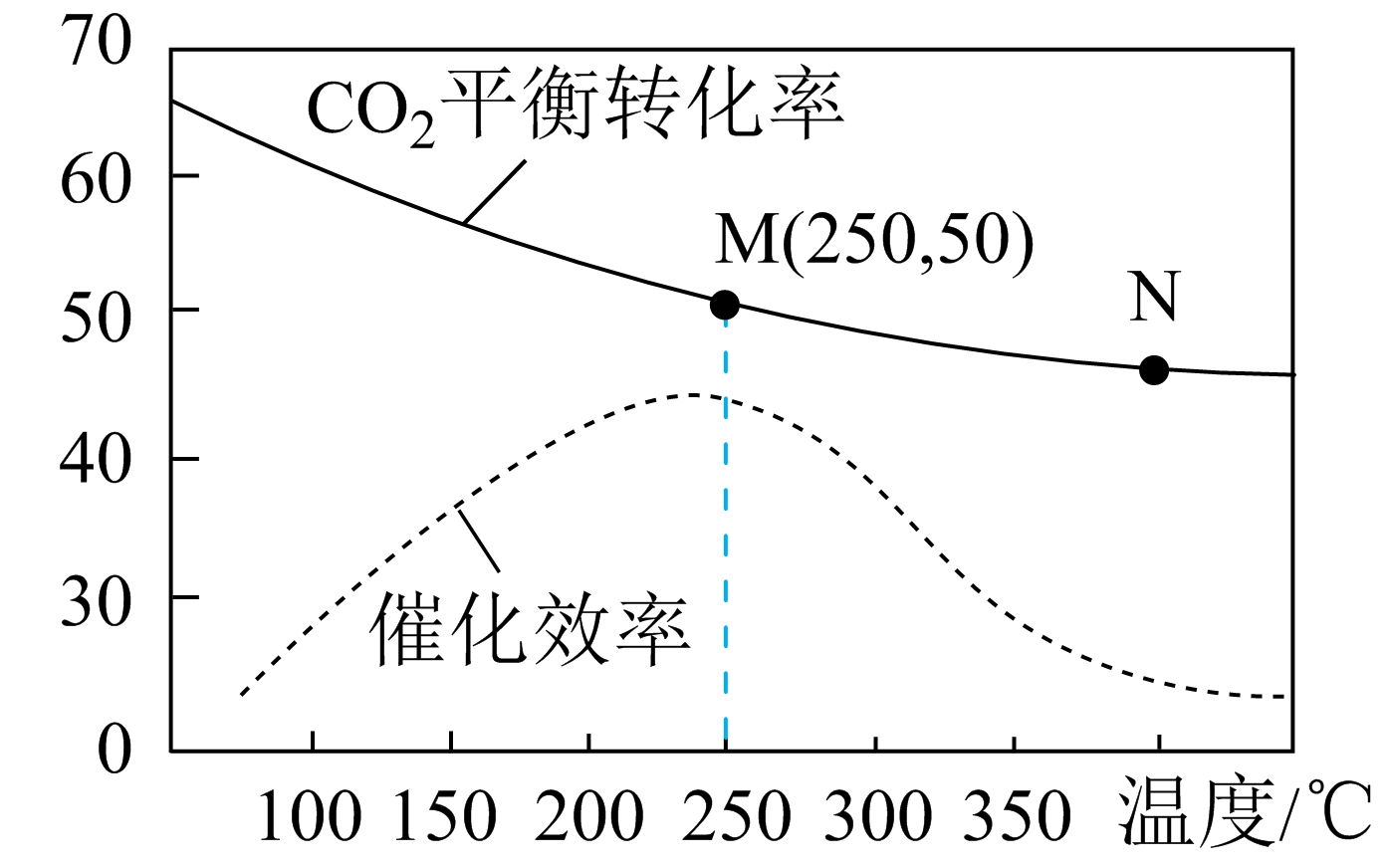
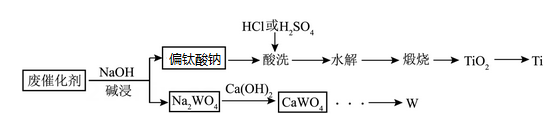
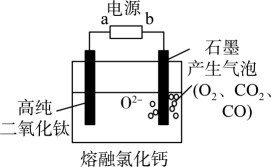
1.某同学利用简易量热计测量放热反应 的焓变
的焓变 (忽略温度对焓变的影响),实验结果见下表:
(忽略温度对焓变的影响),实验结果见下表:
序号 | 反应试剂 | 体系温度 | ||
反应前 | 反应后 | |||
i |
|
| a | b |
ii |
| a | c | |
溶液比热容取 , 溶液的密度取
, 忽略溶液体积、质量变化以及水以外各物质吸收的热量.下列说法不正确的是( )
A.
简易量热计中含有温度计、玻璃搅拌器
B.
温度: C.
实验i反应放出的热量为:
C.
实验i反应放出的热量为: D.
根据实验ii,可得
D.
根据实验ii,可得
【考点】
反应热和焓变;