1.回答下列问题:
(1)
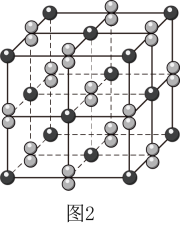
①金刚砂的主要成分的化学式是。
(2)
 分子的空间结构为,共价键为键(填“极性”或“非极性”)
(3)
比较还原性强弱:
分子的空间结构为,共价键为键(填“极性”或“非极性”)
(3)
比较还原性强弱:
 (填“>”“<”或“=”);用一个离子方程式说明与
(填“>”“<”或“=”);用一个离子方程式说明与 与
与 的还原性相对强弱。
(4)
科学家已获得了气态
的还原性相对强弱。
(4)
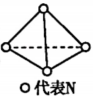
科学家已获得了气态 分子,其结构为正四面体。已知断裂1molN-N吸收193kJ能量,断裂1molN≡N吸收946kJ能量,则
分子,其结构为正四面体。已知断裂1molN-N吸收193kJ能量,断裂1molN≡N吸收946kJ能量,则 完全转化为
完全转化为 时(填“吸收”或“放出”)能量
时(填“吸收”或“放出”)能量
【考点】
判断简单分子或离子的构型;
极性分子和非极性分子;
氧化还原反应;
吸热反应和放热反应;
能力提升
真题演练