1.
(1)
Ⅰ.页岩气中含有 、
、 、
、 等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的
等气体,是可供开采天然气资源。页岩气的有效利用需要处理其中所含的 和
和 。
。
 和
和 在Cu/ZnO催化下发生反应可合成清洁能源甲醇:
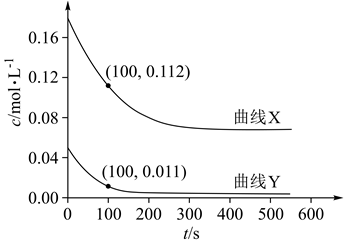
在Cu/ZnO催化下发生反应可合成清洁能源甲醇: , 该反应实际上分两步进行。
, 该反应实际上分两步进行。
(2)
可利用 热分解制备
热分解制备 , 已知下列反应的热化学方程式:
(3)
, 已知下列反应的热化学方程式:
(3)
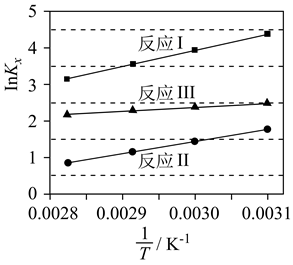
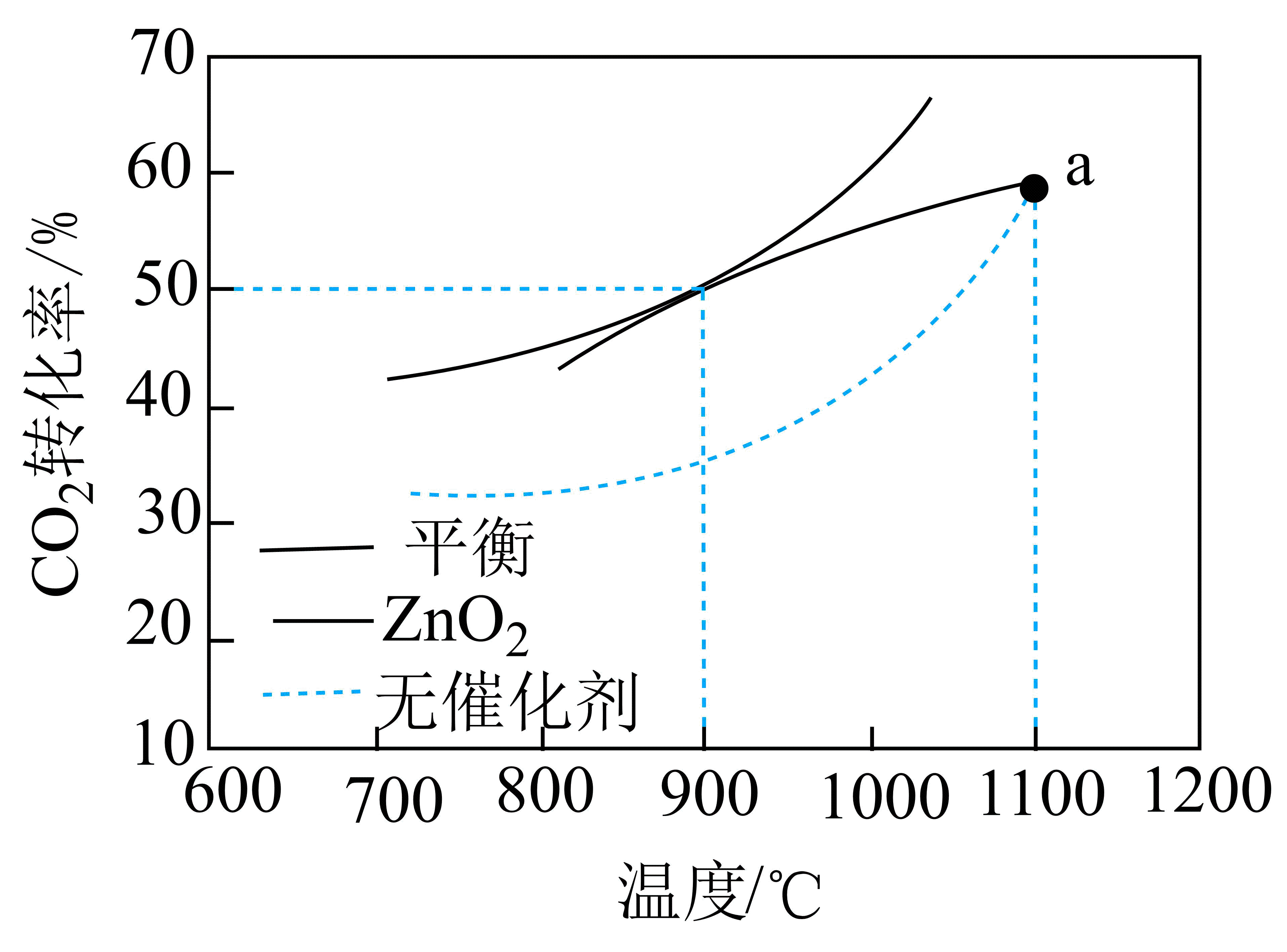
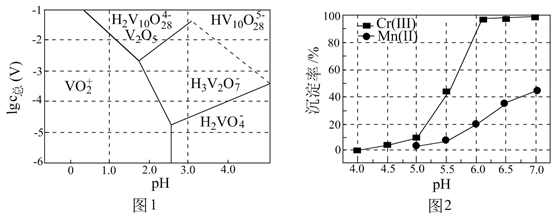
 重整技术是实现“碳中和”的一种理想的
重整技术是实现“碳中和”的一种理想的 利用技术,反应为:
利用技术,反应为: 。在pMPa时,将
。在pMPa时,将 和
和 按物质的量之为1:1:充入密闭容器中,分别在无催化剂及
按物质的量之为1:1:充入密闭容器中,分别在无催化剂及 催化下反应相同时间,测得
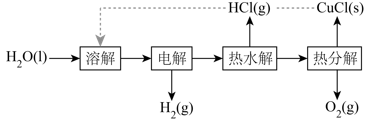
催化下反应相同时间,测得 的转化率与温度的关系如图所示:
(4)
Ⅱ.回收利用工业废气中的
的转化率与温度的关系如图所示:
(4)
Ⅱ.回收利用工业废气中的 和
和 , 实验原理示意图如下。
, 实验原理示意图如下。
断开(或形成)1mol化学键的能量变化数据如下表所示,利用下表中的数据可知,该反应每生成1mol甲醇,需要(填“吸收”或“放出”)kJ的热量。
化学键 | H-H | C-O | C=O | O-H | C-H |
436 | 326 | 803 | 464 | 414 |
①
②
③
计算热分解反应④
。
在pMPa、900℃、催化条件下,将
、
、
按物质的量之比为
充入密闭容器,
的平衡转化率为
, 此时平衡常数
(以分压表示,分压=总压×物质的量分数;写出含
、
、
的计算表达式)。
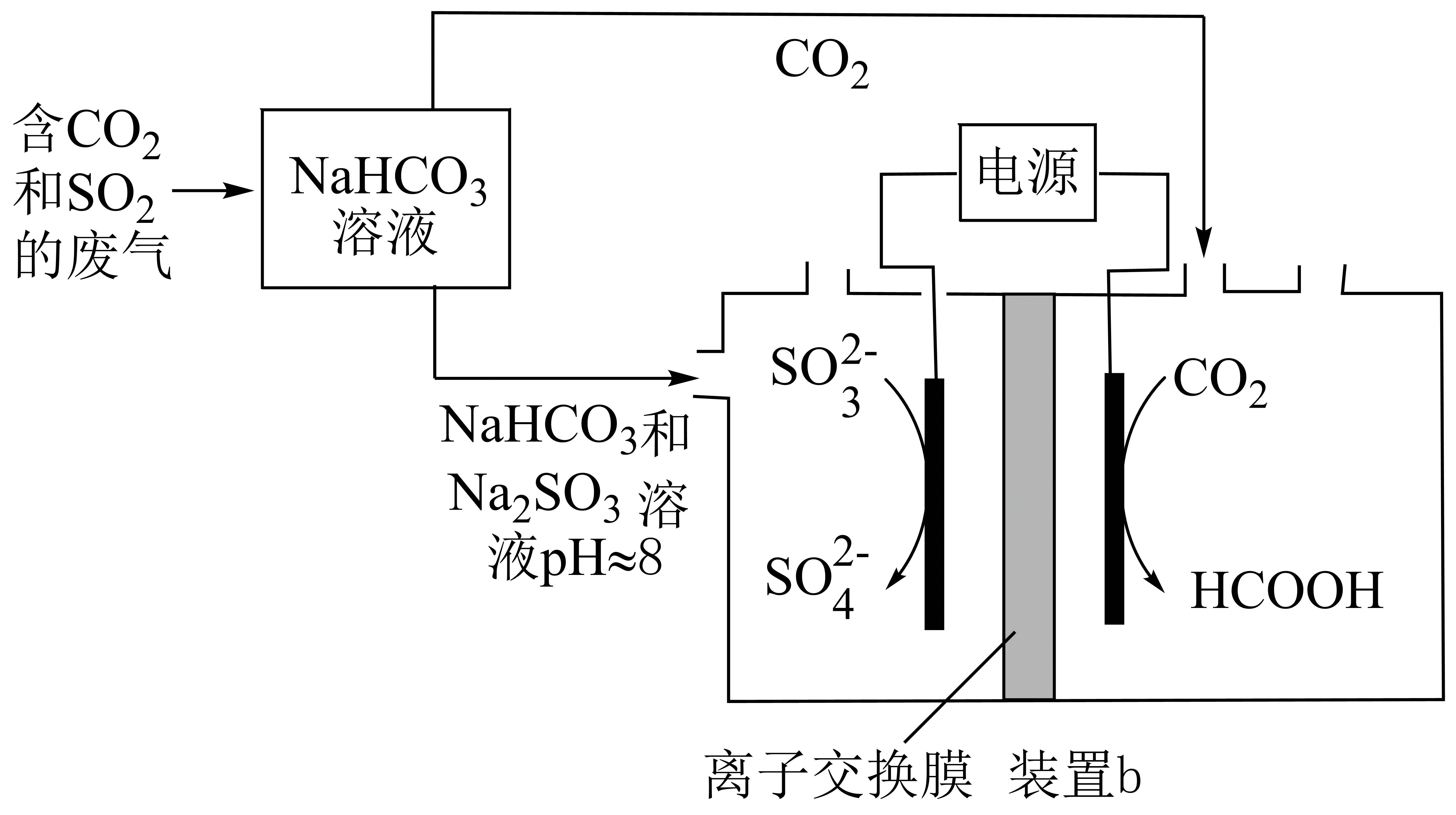
①装置b中参与反应的电极为极(填“正”、“负”、“阴”或“阳”)
②反应后装置b中溶液pH变化(填“增大”、“减小”或“不变”)
③装置b中的总反应的离子方程式为。
【考点】
盖斯定律及其应用;
电极反应和电池反应方程式;
化学平衡转化过程中的变化曲线;
化学平衡的计算;
电解池工作原理及应用;
能力提升
真题演练










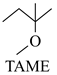 △H1
△H1 △H2
△H2