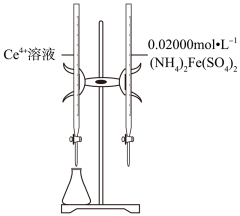
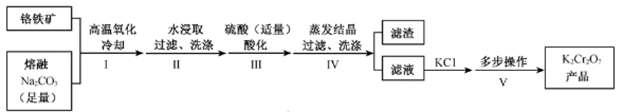
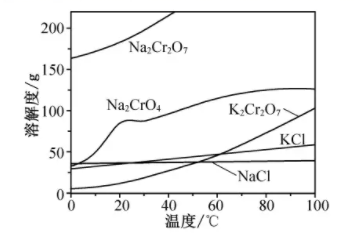
1.碘化钠在医药中用作甲状腺肿瘤防治剂、祛痰剂和利尿剂,也用作食品添加剂、感光剂等。工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下:
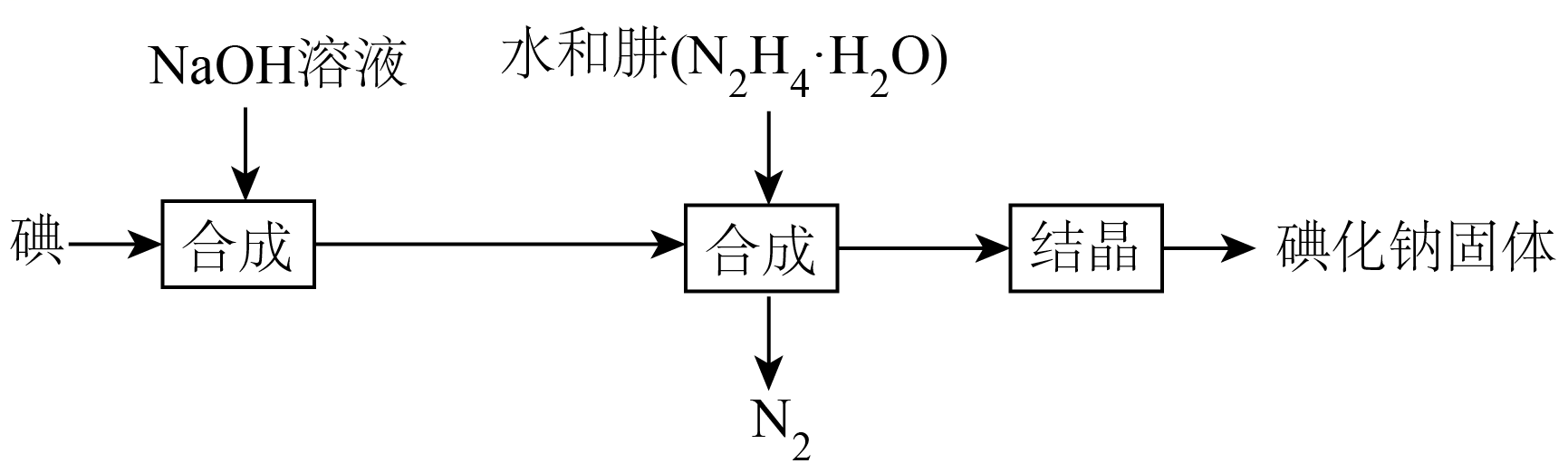
已知:在100℃以上分解。
(1)
已知:在合成过程的反应产物中含有NaIO3 , 则在合成过程中消耗了3molI2 , 所生成NaIO3的物质的量为mol。
(2)
写出还原过程中的离子方程式;在还原过程中,为了加快反应,可采取可提高反应温度,但温度不得超过℃;请选择下列试剂检测所得碘化钠固体中是否含有NaIO3杂质(选填字母)。
(3)
测定产品中NaI含量的实验步骤如下:
(4)
碘化钠固体的保存方法是。
A.FeCl2溶液 B.冰醋酸 C.KI溶液 D.淀粉溶液
a.称取4.000g样品、溶解,在250mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入淀粉溶液作指示剂;
c.用的Na2S2O3溶液进行滴定至终点(发生反应的方程式为:
),重复测定2次,所得的相关数据如下表:
测定序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
1 | 25.00 | 006 | 24.04 |
2 | 25.00 | 0.02 | 24.02 |
3 | 25.00 | 0.12 | 24.14 |
①操作b中,加入足量的FeCl3溶液时所发生的离子方程式为。
②滴定终点观察到的现象为。
③计算该样品中NaI的含量为。(只写出有具体数值的表达式即可)
【考点】
探究物质的组成或测量物质的含量;
制备实验方案的设计;
能力提升
真题演练
 回答下列问题:
回答下列问题: