1.合成氨所需的H2可由反应CO(g)+H2O(g)=CO2(g)+H2(g) ∆H<0提供,下列措施中,能提高CO转化率的是( )
A.
增大水蒸气浓度
B.
升高温度
C.
增大CO浓度
D.
增大压强
【考点】
化学平衡的影响因素;
化学平衡移动原理;
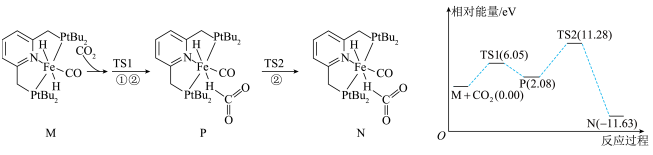




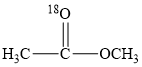 +OH-
+OH- 
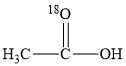 +CH3O-能量变化如图所示。已知
+CH3O-能量变化如图所示。已知 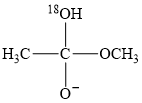 为快速平衡,下列说法正确的是( )
为快速平衡,下列说法正确的是( ) 