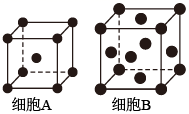
1.科学家模拟光合作用,利用太阳能制备甲烷和异丙醇等燃料。
(1)
利用一种新型高效二元铜铁催化剂,在光照条件下,将 、
、 转化为
转化为 。
(2)
某光电催化反应器如图所示,利用电化学原理模拟光合作用由
。
(2)
某光电催化反应器如图所示,利用电化学原理模拟光合作用由 制异丙醇。
制异丙醇。
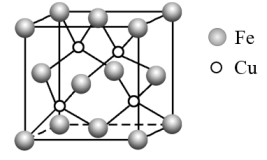
①目前测定晶体结构可靠的科学方法是。一种铜铁催化剂的晶胞如图所示,基态原子的电子排布式为,该晶胞中与一个
原子相紧邻的
原子有个。
②在光照和铜铁催化剂条件下,基态碳原子吸收能量变为激发态原子。下列3种不同状态的碳原子轨道表示式中,能量状态最高的是(填字母)。
a.
b.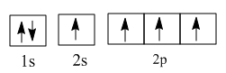
c.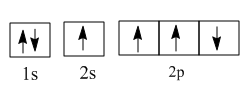

①已知Ti元素的电负性为1.5,O元素的电负性为3.5,则、O原子之间通过键形成稳定的化合物。
②电极表面生成异丙醇的电极反应式为,此电极反应需选用高活性和高选择性的电化学催化剂,其目的是。
【考点】
原子核外电子排布;
原子核外电子的运动状态;
电极反应和电池反应方程式;
电解池工作原理及应用;
能力提升
真题演练
 )易与Cu2+结合生成化合物II(
)易与Cu2+结合生成化合物II( )。请回答:
)。请回答: