一、选择题:(共16题,共48分)
9.把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,首先观察到溶液变红的区域是( )
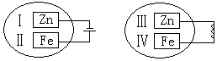
A.
Ⅰ和Ⅲ附近
B.
Ⅱ和Ⅲ附近
C.
Ⅰ和Ⅳ附近
D.
Ⅱ和Ⅳ附近
二、非选择题(共5题,共27分)